HORIBA Scientific poursuit et étend le domaine d’utilisation de sa nouvelle méthode d’analyse pour la détermination de l’empreinte moléculaire de solutés - la méthode A-TEEM (Absorption-Transmission Excitation Emission Fluorescence Matrix) - à l’analyse et à la caractérisation de protéines thérapeutiques.
Récemment introduite pour l’analyse de l’eau, la méthode A-TEEM repose sur l’utilisation de notre spectrofluorimètre rapide, l’AQUALOG, permettant la mesure combinée des signaux de fluorescence et d’absorption - et sur l’analyse multi-variée (chimiométrique) des matrices d’absorption et de fluorescence (EEM).
Cette Méthode est ici appliquée à la caractérisation de différents types d’insulines thérapeutiques utilisées dans les traitements des diabètes. Mais la méthode A-TEEM est universelle et peut être utilisée pour caractériser toute autre solution biologique complexe tels que les vaccins, les mélanges de protéines, d’enzymes et mêmes les cultures cellulaires.
Aujourd’hui, il existe de nombreuses préparations d’insulines qui seront injectées en fonctions des types de diabètes. On différencie ainsi :
• L’insuline humaine produite naturellement par le pancréas
• Les insulines rapides et ultrarapides
• Les insulines dites lentes dont les effets se font sentir plus lentement
Les différentes insulines ont pu rapidement être discriminées par la méthode A-TEEM. L’analyse chimiométrique décompose les solutions d’insulines en 4 composantes principales dont les contributions varient d’un type à l’autre. Ainsi, l’insuline de type « lente » (glargine) qui est séquencée pour produire des agrégats et avoir une solubilité plus lente, est caractérisée par une très forte contribution de la composante 3 (tyrosine), bien plus élevée que les contributions de cette même composante 3 observées pour les insulines humaine et « rapide » (aspart) qui sont moins favorables à l’agrégation.
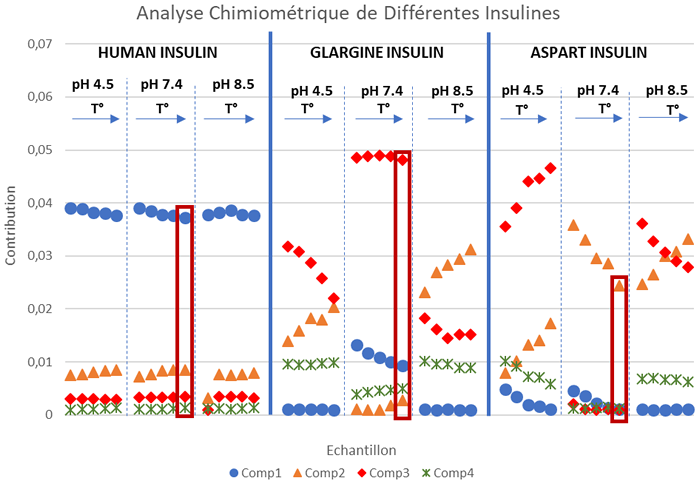
Figure #1 : Contribution des composantes obtenues par l’analyse chimiométrique multi-variée de trois types d’insulines (4mg/mL): insuline humaine (gauche), insuline-glargine de type lente (centre), insuline-aspart de type rapide (droite), toutes disponibles commercialement. Chaque échantillon est testé pour trois pH différents (4.5, 7.4 et 8.5) et pour à cinq points de température différents (de gauche à droite : 5, 20, 25, 30 et 37°C). Les conditions biologiques standard – 37°C et pH 7.4 – sont encadrées en rouge.
Pour plus d’informations sur l’AQUALOG et la méthode A-TEEM et sur son utilisation pour la caractérisation de l’insuline :
https://static.horiba.com/fileadmin/Horiba/Application/Health_Care/Human_Health_Care/Insulin_Structure_and_Stability-ATEEM_LR.pdf
https://doi.org/10.1088/2050-6120/aaa818