Par Sino Biological - www.sinobiological.com
Introduction
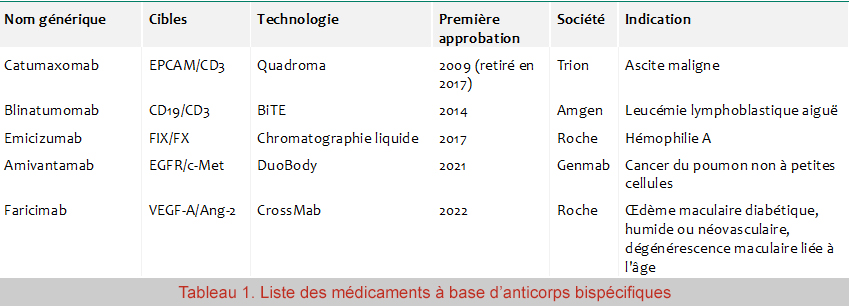
Les anticorps monoclonaux (AcM) sont des agents thérapeutiques importants pour le traitement de nombreuses maladies humaines telles que le cancer, les maladies auto-immunes, les maladies cardiovasculaires, l'asthme et les infections virales. Contrairement aux AcM monospécifiques, les anticorps bispécifiques (bsAbs) sont des anticorps contenant deux sites de liaison à l'antigène et peuvent donc cibler simultanément deux épitopes différents. En janvier 2022, le faricimab (Vabysmo, Roche) a été approuvé par la FDA pour traiter la dégénérescence maculaire liée à l'âge (DMLA) humide et l'œdème maculaire diabétique (OMD). Outre le retrait du premier bsAb Catumaxomab en 2017, il s'agit du 4ème médicament à bsAbs actuellement sur le marché (tableau 1). Avec une attention accrue portée au domaine des anticorps, les bsAbs représentent près de 20% du pipeline d'anticorps cliniques, avec environ 160 bsAbs actuellement en essais cliniques.
Conception et ingénierie des anticorps bispécifiques
Dans un premier temps, des bsAbs ont été produits par la méthode du quadrome (hybride d'hybridome). En raison de l'assemblage aléatoire de deux chaînes lourdes et deux chaînes légères différentes, il n'existe qu'un seul bsAb fonctionnel, les neuf autres variants sont soit non fonctionnels soit monospécifiques. Cela conduit à un faible rendement des bsAbs cibles, ce qui pose un problème majeur pour le processus de purification en aval.
Pour surmonter le problème de l'association des chaînes lourdes et légères, les scientifiques se sont concentrés sur la technologie de l'ADN recombinant pour concevoir des bsAbs. Sur la base de leurs différentes propriétés, les bsAbs sont classés en deux types distincts : Les bsAbs de type IgG et non-IgG. Les bsAbs de type IgG possèdent un domaine constant d'immunoglobuline conservé, ce qui leur permet de conserver les fonctions effectrices médiées par le fragment Fc, comme dans les cas de La cytotoxicité dépendante du complément (CDC) et La cytotoxicité à médiation cellulaire dépendante des anticorps (ADCC). En raison de leur poids moléculaire élevé, ils ont également une longue demi-vie dans le sérum, une meilleure solubilité et une plus grande stabilité. D'autre part, en raison de l'absence de fragments Fc, les bsAbs de type non-IgG ont une taille plus petite, une immunogénicité plus faible, une demi-vie plus courte dans le sérum, mais une meilleure pénétration tissulaire.
Anticorps bispécifiques de type IgG
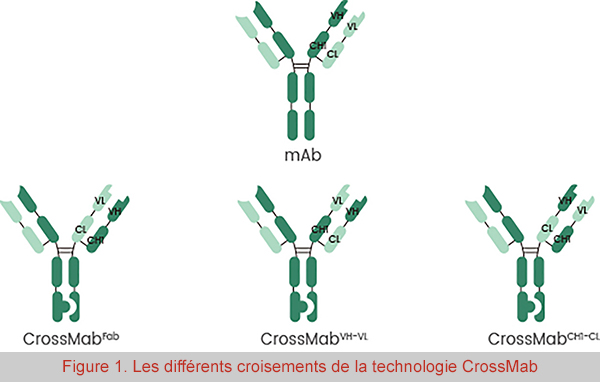
L'homodimérisation des deux chaînes lourdes des IgG est réalisée par l'interaction entre les domaines CH3. Pour résoudre le problème de mésappariement des chaînes lourdes, différentes technologies peuvent être appliquées pour modifier le domaine CH3 en vue de l'hétérodimérisation des fragments Fc. L'approche « knobs-into-holes » (KiH), littéralement « nœud dans la cavité », a été proposée pour la première fois dans les années 1990 et a été largement utilisée pour l'ingénierie des fragments Fc. Elle consiste à remplacer un grand acide aminé par un petit dans le domaine CH3 (le « nœud ») d'un anticorps et vice versa (la « cavité ») dans l'autre anticorps. L’approche alternative telle que SEEDbody est également utilisée pour générer des anticorps bispécifiques hétérodimériques. Par ailleurs, il est également essentiel de résoudre le problème de mésappariement des chaînes légères, et l'approche CrossMab est l'une de ces technologies. Comme le montre la figure 1, les trois principaux formats de CrossMAb sont CrossMabFab, CrossMabVH-VL et CrossMabCH1-CL. En échangeant les régions de la chaîne lourde et légère d'un côté, la chaîne légère de BsAb peut être assemblée correctement. Pour minimiser les erreurs de mésappariement, cette méthode est généralement associée à d'autres approches telles que KiH, DEEK et ART-Ig. En combinant le KiH et le CrossMab, Roche a mis au point un produit phare, le Faricimab, qui présente une double spécificité pour l'Ang-2 et le VEGFA.
Anticorps bispécifiques de type non-IgG
La conception d'anticorps bispécifiques de type non-IgG est relativement simple. Les fragments scFv sont largement utilisés comme éléments de base pour générer des anticorps bispécifiques. En utilisant des lieurs peptidiques correctement conçus, les fragments scFv peuvent former des dimères, trimères, tétramères, pentamères et même des oligomères d'ordre supérieur. L'engageur de cellules T bispécifique (BiTE) est un type de fragment scFv en tandem qui consiste en deux fragments scFv dont l'un se lie au CD3 sur les cellules T et l'autre se lie à un antigène de surface sur les cellules tumorales pour orienter les cellules T vers la destruction des cellules tumorales. Grâce à cette approche, le Blinatumomab (Blincyto) a été approuvé par la FDA pour le traitement de la leucémie lymphoblastique aiguë (LLA). Les autres formats usuels sont les protéines de reciblage à double affinité (DART), les diacorps en tandem (TandAbs), les diacorps à chaîne unique, les DNL (dock-and-lock) et les nanocorps.
Expression et production d'anticorps bispécifiques
Le choix des systèmes d'expression appropriés est essentiel pour l'expression et la production efficaces d'anticorps bispécifiques. Certains anticorps bsAbs de type non-IgG, tels que les BiTE et les fragments scFv bispécifiques en tandem peuvent être exprimés dans des levures ou des cellules de mammifères comme les cellules CHO et HEK293. Les bactéries constituent un choix courant pour l'expression des scFv car elles peuvent se développer rapidement dans des milieux de bon marché et produire des protéines hétérologues en grandes quantités. Cependant, les molécules scFv exprimées n'ont pas la possibilité de former des liaisons disulfures intra-domainequi est essentiel à la structure du « pli de l'immunoglobuline ». Des étapes supplémentaires de repliage et de récupération des protéines sont généralement nécessaires pour générer des molécules scFv solubles. Pour résoudre ces problèmes, les cellules de mammifères peuvent être utilisées pour exprimer des scFv bispécifiques grâce à leur capacité à effectuer des modifications post-traductionnelles complexes. Comme elles sont dépourvues de la région Fc, elles sont généralement purifiées en utilisant une chromatographie His-tag ou protéine L.
Comme les AcM classiques, les bsAbs de type IgG sont exprimés principalement dans les cellules de mammifères, notamment dans les cellules CHO. Cependant, la production de bsAbs est plus difficile en raison du double nombre de gènes de chaînes lourdes et légères. En général, il faut au moins deux plasmides d'expression soient co-transfectés dans les cellules CHO. De plus, le rapport entre les deux plasmides peut également influencer à la fois la qualité et la quantité des bsAbs exprimés. Au cours des premiers stades du développement de bsAb, les cellules HEK293 sont souvent utilisées pour l'expression transitoire. Il est parfois difficile d'augmenter l'expression transitoire d'IgG et les titres d'anticorps sont relativement faibles par rapport aux cellules CHO stables. En raison des diverses similitudes structurelles entre les anticorps monoclonaux et bispécifiques, de nombreux procédés de purification établis pour les AcM classiques sont compatibles avec les bispécifiques. Diverses méthodes sont employées pour la purification des bsAbs telles que la puriification par affinité, ionqiue, d’exclusion de taille, d’hydrophobie et les techniques de séparation basées sur des modes mixtes.
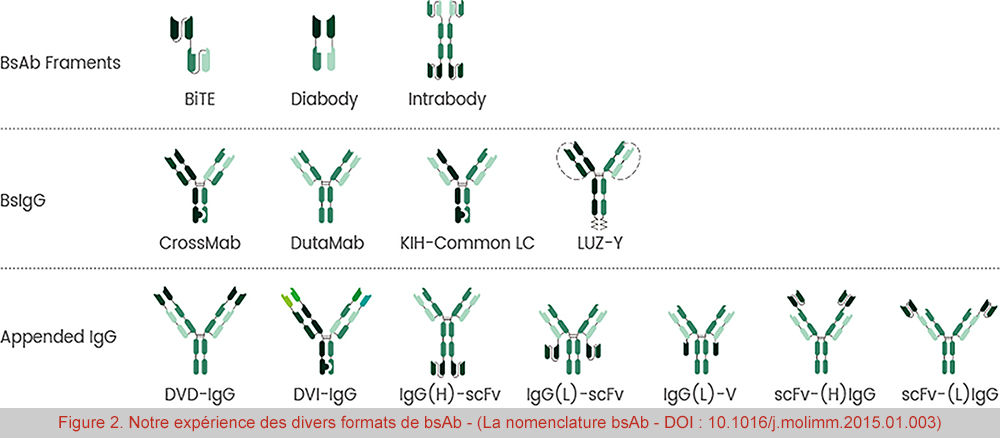
Comprenant ces défis de fabrication, Sino Biological fournit des services d'expression d'anticorps bispécifiques rapides et efficaces basés sur notre expertise et notre expérience dans l'expression des cellules de mammifères. À partir de la séquence de l'anticorps, nous pouvons fournir plusieurs formats de bsAb tels que BiTE, Diabody, CrossMab et DVD-IgG (certains formats sont énumérés dans la figure 2). Nous avons achevé de nombreux projets de production de bsAb avec des taux de réussite globaux supérieur à 90% et le rendement le plus élevé atteignant approximativement 250mg/L.
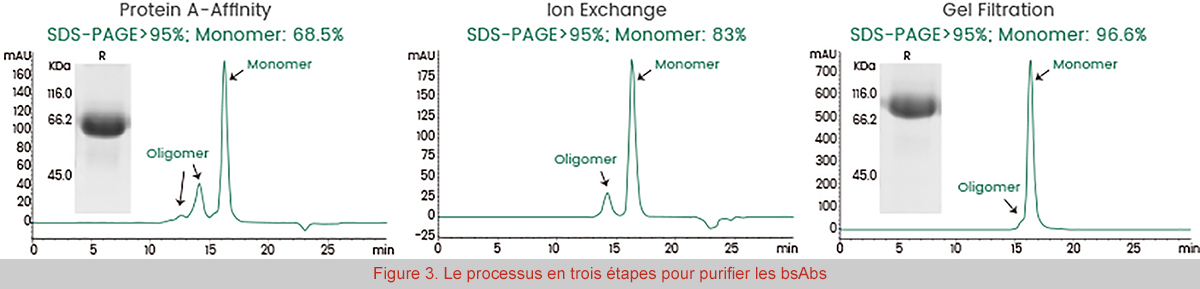
Nous présentons ici un cas particulier de production d'anticorps bispécifiques. La chaîne lourde de la construction bsAb présente un motif de knobs-in-holes (KiH), ou nœud dans la cavité. Après le processus de purification en trois étapes (figure 3), la pureté du monomère est passée de 68,5 % à 96,6 %, répondant ainsi aux exigences finales du contrôle qualité.
Remarques finales
Grâce au développement rapide de la technologie de l'ADN recombinant et à une connaissance approfondie de l'ingénierie des anticorps, divers formats d'anticorps bispécifiques sont développés afin de poursuivre une activité biologique et des objectifs cliniques optimaux. Les anticorps bispécifiques ont déjà montré un grand potentiel thérapeutique dans le traitement du cancer et d'autres maladies comme le diabète, la maladie d'Alzheimer et les maladies ophtalmologiques. Actuellement, de nombreux bsAbs entrent en phase de développement clinique et on peut estimer qu’il y aura plus d’bsAbs autorisés sur le marché dans l'avenir.